Class 12 Chemistry Chapter 3 Important Questions Answers
प्रश्न -1. अभिक्रिया के वेग से आप क्या समझते हैं? समझाइए l
अथवा
Also Read
अभिक्रिया के वेग का अर्थ उदाहरण सहित स्पष्ट कीजिए।
उत्तर : वह दर, जिस पर समय के साथ-साथ अभिकारक पदार्थों का सान्द्रण परिवर्तित होता है, अभिक्रिया का वेग कहलाता है।
यदि सूक्ष्म अन्तराल dt में अभिकारक के dx मोल उत्पाद में परिवर्तित होते हों, तो
अभिक्रिया का वेग यदि अन्तराल dt में अभिकारक के dc मोल शेष रहते हों, तो अभिक्रिया का वेग = (dx)/(dt) = – (d[C])/(dt)
प्रश्न -2- तात्क्षणिक वेग क्या है? आप इसे कैसे ज्ञात करे?
[2 marks important]
उत्तर: किसी निश्चित क्षण पर अभिक्रिया का वास्तविक वेग उसका तात्क्षणिक वेग कहलाता है। अभिक्रिया के तात्क्षणिक वेग को समय और सान्द्रता के मध्य खींचे गए ग्राफ की सहायता से भी ज्ञात करते हैं। समय व सान्द्रता के मध्य खींचे गए ग्राफ में किसी विशिष्ट समय और विशिष्ट सान्द्रता के संगत बिन्दु पर खींची गई स्पर्श रेखा का ढाल (slope), अभिक्रिया के तात्क्षणिक वेग को प्रदर्शित करता है।
इस प्रकार, जिस क्षण पर अभिक्रिया का तात्क्षणिक वेग ज्ञात किया जाना है, वक्र पर उससे सम्बन्धित बिन्दु पर एक स्पर्श रेखा खींचकर उसकी ढाल से अभिक्रिया का तात्क्षणिक वेग ज्ञात हो जाता है।
प्रश्न -3- अभिक्रिया की कोटि का अर्थ उदाहरण सहित स्पष्ट कीजिए।
[Important questions]
उत्तर : किसी रासायनिक अभिक्रिया में उपस्थित अभिकारक अणुओं की वह संख्या जिसका सान्द्रण रासायनिक परिवर्तन के परिणामस्वरूप परिवर्तितं होता है, अभिक्रिया की कोटि कहलाती है। यह प्रायोगिक रूप से निर्धारित अभिक्रिया दर समीकरण में सान्द्रता के पदों की संख्या के बराबर होती है।
उदाहरण– अभिक्रिया –
nA+m → उत्पाद
के लिए वेग व्यंजक निम्न है-
दर = k [A] ^ x [B] ^ y
अतः इस अभिक्रिया की कोटि = x + y
x तथा y का मान n तथा m के समान भी हो सकता है और उससे भिन्न भी।
प्रश्न 4-. शून्य कोटि की अभिक्रिया को उदाहरण द्वारा समझाइए।
[ 2026 Expected]
उत्तर : वह अभिक्रिया जिसकी प्रगति में अभिकारक के किसी भी अणु का सान्द्रण परिवर्तित नहीं होता है अर्थात् जिसका वेग अभिकारक के सान्द्रण पर निर्भर नहीं करता है, शून्य कोटि की अभिक्रिया कहलाती है।
माना कि कोई अभिक्रिया निम्नलिखित प्रकार से होती है-
A→B+C
यदि इसका वेग × [A] ^ 0 हो तो यह शून्य कोटि की अभिक्रिया होगी। उदाहरण-सूर्य के प्रकाश की उपस्थिति में H{2} व Cl{2} का संयोग –
H2 + Cl2 सूर्य का प्रकाश →2HCl
प्रश्न 5- प्रथम कोटि की अभिक्रिया के चार प्रमुख अभिलक्षण लिखिए।
उत्तर : प्रथम कोटि की अभिक्रिया के अभिलक्षण-
(1) प्रथम कोटि की अभिक्रिया में अभिकारक पदार्थ का आधा सान्द्रण परिवर्तित होने में लगने वाला समय, अभिकारक पदार्थ के प्रारम्भिक सान्द्रण पर निर्भर नहीं करता है। इन अभिक्रियाओं ३० अर्द्ध-आयुकाल वेग स्थिरांक के व्युत्क्रमानुपाती होता है।
(2) प्रथम कोटि की अभिक्रिया के पूर्ण होने में अनन्त समय लगता है।
(3) प्रथम कोटि की अभिक्रिया के लिए समाकलित वेग समीकरण निम्नलिखित है-
k = 2.303/t [log(a/(a – x)
(4) प्रथम कोटि की अभिक्रिया के वेग स्थिरांक की इकाई समय -1 होती है।
प्रश्न 6- कैसे अभिक्रिया गति प्रभावित होती है-
(i) अभिकारक सान्द्रण के परिवर्तन पर?
(ii) ताप के परिवर्तन पर?
(iii) उत्प्रेरक की उपस्थिति पर?
अथवा अभिक्रिया की दर पर तापमान और दाब के प्रभाव को समझाइए।
उत्तर : (i) अभिकारक सान्द्रण का प्रभाव- अभिकारक का सान्द्रण बढ़ने पर अभिकारकों के अणुओं की संख्या में वृद्धि हो जाती है, जिसके फलस्वरूप उन अणुओं की प्रभावी टक्करों की संख्या में वृद्धि के कारण अभिक्रिया गति में भी वृद्धि हो जाती है। अतः अभिकारक का सान्द्रण बढ़ने पर अभिक्रिया गति में वृद्धि होती है।
(ii) तापमान का प्रभाव अभिक्रिया का तापमान बढ़ने के साथ अभिक्रिया की दर में वृद्धि होती है, क्योंकि तापमान वृद्धि पर अभिकारकों के अणुओं की इकाई समय में संघट्टों (collisions) की संख्या में वृद्धि हो जाती है।
(iii) उत्प्रेरक का प्रभाव – उत्प्रेरक के द्वारा अभिक्रिया दर को प्रभावित करने का कारण संघट्टवाद के द्वारा समझाया गया है, क्योंकि उत्प्रेरक रासायनिक अभिक्रिया में भाग लेकर अभिकारकों के साथ अस्थायी आबन्ध बनाता है, जो मध्यवर्ती संकर में परिवर्तित होता है, जो बहुत कम स्थायी होता है और वियोजित होकर उत्पाद व उत्प्रेरक देता है, ऐसा माना जाता है परन्तु क्रियाविधि के आधार पर उत्प्रेरक सक्रियित संकर बनाने हेतु आवश्यक सक्रियण ऊर्जा का मान कम कर देता है, फलस्वरूप अभिक्रिया कम ताप पर ही तीव्र गति से होने लगती है।
अभिक्रिया दर × 1/ सक्रियण ऊर्जा
(iv) दाब का प्रभाव – गैसीय अभिकारकों के अणुओं पर दाब बढ़ाने पर उनके अणु परस्पर निकट आ जाते हैं, क्योंकि उनका आयतन घट जाता है। अतः इकाई आयतन में उनका सान्द्रण बढ़ जाता है, जिससे अणुओं की संख्या में वृद्धि हो जाती है। इसके परिणामस्वरूप अणुओं की प्रभावी टक्करों (effective collisions) की संख्या भी बढ़ जाती है और अभिक्रिया की दर बढ़ जाती है।
प्रश्न 7- अभिक्रिया की आण्विकता तथा कोटि में क्या अन्तर है? एक उदाहरण देकर स्पष्ट कीजिए।
अथवा
आण्विकता (अणुसंख्यता) तथा अभिक्रिया की कोटि में अन्तर स्पष्ट कीजिए।
उत्तर : अभिक्रिया की आण्विकता तथा कोटि में अन्तर
(1) अभिक्रिया की आण्विकता सदैव एक पूर्ण संख्या होती है, जबकि अभिक्रिया की कोटि भिन्नात्मक भी हो सकती है।
(2) अभिक्रिया की आण्विकता कभी-भी शून्य नहीं हो सकती, जबकि अभिक्रिया की कोटि शून्य भी हो सकती है।
(3) किसी अभिक्रिया की आण्विकता और कोटि समान या भिन्न-भिन्न हो सकती हैं।
(4) आण्विकता अभिक्रिया के पद में उपस्थित भाग लेने वाले अणुओं की संख्या है, परन्तु अभिक्रिया की कोटि अभिक्रिया के वेग और अभिकारकों की सान्द्रता में सम्बन्ध बताती है।
(5) अभिक्रिया के वेग निर्धारक पद में भाग लेने वाले अणुओं की संख्या उस पद की आण्विकता कहलाती है। अभिक्रिया की कोटि उन अणुओं की संख्या है, जिनकी सान्द्रताएँ अभिक्रिया के वेग को निर्धारित करती हैं।
(6) अभिक्रिया की आण्विकता की व्याख्या उसकी क्रियाविधि द्वारा करते हैं, जबकि अभिक्रिया की कोटि प्रयोगों द्वारा निकाली जाती है।
उदाहरण – आण्विकता और कोटि में अन्तर निम्नलिखित उदाहरणों द्वारा स्पष्ट हो जाता है-
(i) CH3COOC2H5 + NaOH → CH3COONa
+ C2H5OH
(ii) CH3COOC2H5 +H2O. H+→ CH3COOH + C2H5OH
अभिक्रियाएँ (i) तथा (ii) दोनों द्वि-अणुक हैं। अभिक्रिया (i) द्वितीय कोटि की अभिक्रिया है, क्योंकि इस अभिक्रिया का वेग CH3COOC2H5 और NaOH दोनों के सान्द्रण पर निर्भर करता है, जबकि अभिक्रिया (ii) प्रथम कोटि की अभिक्रिया है, क्योंकि इस अभिक्रिया का वेग केवल CH3COOC2H5 के सान्द्रण पर निर्भर करता है।
प्रश्न 8 – किसी रासायनिक अभिक्रिया का औसत वेग और तात्क्षणिक वेग से आपका क्या तात्पर्य है? अभिक्रिया के वेग पर ताप के प्रभाव को संक्षेप में समझाइए।
उत्तर – औसत वेग-किसी रासायनिक अभिक्रिया में उपस्थित अभिकारक या उत्पाद के सान्द्रण में प्रति इकाई समय में होने वाले परिवर्तन को उस अभिक्रिया का औसत वेग कहते हैं।
औसत वेग = -अभिकारक की सान्द्रता में परिवर्तन/ परिवर्तन में लगा समय
= + उत्पाद की सान्द्रता में परिवर्तन/ परिवर्तन में लगा समय
तात्क्षणिक वेग- किसी निश्चित क्षण पर अभिक्रिया का वास्तविक वेग उसका तात्क्षणिक वेग कहलाता है। यदि किसी अभिक्रिया के अभिकारक और उत्पाद की सान्द्रता परिवर्तन को ∆C और परिवर्तन में लगे समय को ∆t माना जाए तो अभिक्रिया का तात्क्षणिक वेग होगा। = ± (∆C)/(∆t)
अभिक्रिया का वेग- वह दर जिसमें समय के साथ अभिकारक पदार्थ का सान्द्रण परिवर्तित होता है, अभिक्रिया का वेग कहलाता है।
अभिक्रिया के वेग को प्रभावित करने वाले कारक –
1. सान्द्रण का प्रभाव – अभिकारक का सान्द्रण बढ़ने पर अणुओं की
संख्या में वृद्धि के साथ-साथ प्रभावी टक्करों की संख्या में वृद्धि के कारण अभिक्रिया के वेग में वृद्धि होती है।
अभिक्रिया का वेग × उसके अभिकारक का सान्द्रण
अतः अभिकारकों का सान्द्रण बढ़ने से अभिक्रिया का वेग बढ़ेगा और उनका सान्द्रण घटने से अभिक्रिया का वेग घटेगा।
2. ताप का प्रभाव – ताप-वृद्धि पर अभिक्रिया में अभिकारकों के सक्रिय अणुओं की संख्या में वृद्धि हो जाती है फलस्वरूप उनके मध्य प्रभावी टक्करों की संख्या में वृद्धि हो जाती है। इकाई समय में अभिकारक अणुओं की प्रभावी टक्करों की संख्या को, अभिक्रिया का वेग कहते हैं। अतः ताप-वृद्धि पर अभिक्रिया के वेग में वृद्धि होती है। ताप बढ़ाने पर वेग स्थिरांक का मान बढ़ जाता है। 10 deg * C ताप बढ़ने पर वेग स्थिरांक का मान दुगुना या तिगुना हो जाता है। इस कारण भी ताप वृद्धि पर अभिक्रिया का वेग बढ़ता है।
प्रश्न 9- आहींनियस समीकरण दीजिए। अभिक्रिया की सक्रियण ऊर्जा आरेख विधि से कैसे ज्ञात करेंगे ?
उत्तर – अभिकारक अणुओं के संघट्ट से प्राप्त ऊर्जा की वह अतिरिक्त मात्रा जो अभिक्रिया को सम्पन्न कराने के लिए पर्याप्त होती है तथा उसके फलस्वरूप उत्पाद बनते हैं, सक्रियण ऊर्जा कहलाती है।
आहींनियस समीकरण –
k = Ae ^ [(- E_{a}) / RT]—–(1)
जहाँ, k= अभिक्रिया का वेग स्थिरांक,
Ea= अभिक्रिया की सक्रियण ऊर्जा, R→ गैस स्थिरांक, T’ →परम ताप तथा A→ पूर्व-चरघातांकी गुणक या आवृत्ति गुणांक है।
समीकरण (1) का लघुगणक लेने पर,
logek = logeA + [(- E_{a}) / RT] —–(2)
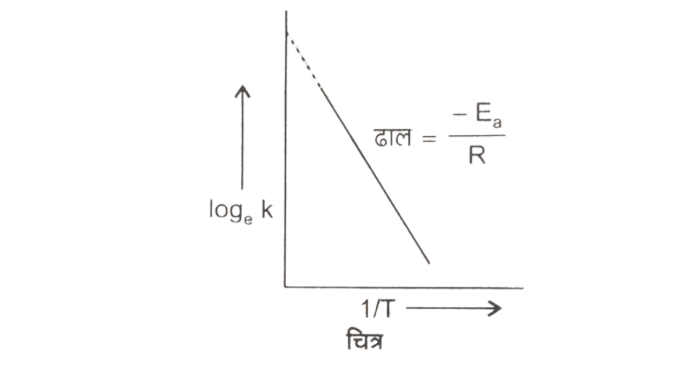
इस आरेख के ढाल की सहायता से Ea का मान ज्ञात कर लेते हैं Ea का मात्रक R के मात्रक पर निर्भर करता है, क्योंकि ढाल का मान = – Ea/R
होता हैं। R का मान रखने पर Ea का मान ज्ञात होता है।
दिए गए समीकरण (2) को निम्न प्रकार से भी लिख सकते हैं-
2.303 log10 k = 2.303 log10 A – Ea/RT
log10k = log10A – Ea/2.303RT
इस समीकरण के आधार पर log 10k व 1/ T’ के मध्य आरेख खींचने पर जो ढाल प्राप्त होता है, उसका मान के बराबर होता है, जिससे -Ea/2.303 सक्रियण ऊर्जा (Ea) का मान ज्ञात कर लेते हैं।

प्रश्न 10- निम्नलिखित पर टिप्पणियाँ लिखिए-
(i) विशिष्ट वेग स्थिरांक
(ii) सक्रियण ऊर्जा।
उत्तर : (i) विशिष्ट वेग स्थिरांक- माना कि किसी रासायनिक अभिक्रिया के किसी क्षण उसके अभिकारक का आण्विक सान्द्रण C हो तो उस समय अभिक्रिया का वेग dx, उसके अभिकारक के सान्द्रण के (dt) समानुपाती होता है, अर्थात्
dx/dt=k.C
,जहाँ एक स्थिरांक है, जिसे वेग स्थिरांक कहते हैं।
यदि C = 1 मोल/लीटर हो तो d/dt (x) = k
अतः स्थिर ताप पर अभिकारक के इकाई सान्द्रण पर अभिक्रिया का वेग उस अभिक्रिया का विशिष्ट वेग स्थिरांक कहलाता है। यह अलग-अलग अभिक्रियाओं हेतु भिन्न-भिन्न होता है तथा इसका मात्रक भी अभिक्रिया की प्रकृति पर निर्भर करता है। इसका मान ताप वृद्धि पर सदैव बढ़ता है।
(ii) सक्रियण ऊर्जा – अभिकारक अणुओं के संघट्ट से प्राप्त ऊर्जा की वह अतिरिक्त मात्रा जो अभिक्रिया को सम्पन्न कराने में पर्याप्त होती है तथा जिसके फलस्वरूप उत्पाद बनते हैं, सक्रियण ऊर्जा कहलाती है। अतः अभिक्रियाओं की औसत स्थितिज ऊर्जा (P.E.) के अतिरिक्त ऊर्जा की वह न्यूनतम मात्रा जो अभिकारक अणुओं के संघट्ट से प्राप्त होती है और अभिकारक अणुओं को उत्पाद में परिवर्तित कर देती है, सक्रियण ऊर्जा कहलाती है।
सक्रियण ऊर्जा = देहली ऊर्जा – अभिकारक अणुओं की औसत स्थितिज ऊर्जा
आहींनियस ने अभिक्रिया के वेग पर ताप के प्रभाव को स्पष्ट करने के लिए एक समीकरण प्रस्तुत की थी, जिसे आहींनियस समीकरण कहा गया जिसके अनुसार,
k= Ae^-Ea/RT
जहाँ A को पूर्व-चरघातांकी गुणक या आवृत्ति गुणांक तथा Ea को सक्रियण ऊर्जा कहते हैं। इसमें अभिक्रिया का वेग स्थिरांक, R गैसीय स्थिरांक तथा T’ परम ताप है।
महत्त्वपूर्ण बिंदु:– U.P बोर्ड परीक्षा में सफल होने के लिए अपने syllabus को अच्छी तरह से समझें और नियमित रूप से अभ्यास करते रहे साथ ही हर विषय पर ध्यान दे